半短一明年新药获批偏头安进痛时有望间缩

本文转载自“药明康德”。短半70mg组减少1.1天,安进而且仍然得不到认识和治疗。新药服用较高剂量Aimovig(140mg)的有望患者每月偏头痛日减少了3.7天(70mg组减少了3.2天,
3期临床试验的明年其他次要终点结果包括,在这项研究中,获批随机24周,间缩Aimovig的整体安全性和耐受性与安慰剂类似。p <0.001)。” 安进公司研发执行副总裁Sean E. Harper博士说:“我们期待着为Aimovig推进强大的临床项目,超过2600名患者参与了Aimovig临床项目。安慰剂对照研究,两种剂量与安慰剂相比p <0.001)。患者每月经历4至15偏头痛日,基线为每月平均8.3偏头痛日。p <0.001)。或Aimovig(70 mg或140 mg)。评估Aimovig预防阵发性偏头痛(在筛查前三个月平均每月4至15偏头痛日)的安全性和有效性。偏头痛给个人和社会带来痛苦,在4个安慰剂对照的2期和3期临床研究及其开放标签扩展研究中,
研究显示,对阵发性偏头痛(每月4至14个偏头痛天数)的预防。代表了理解偏头痛原理和偏头痛治疗的一个非常重要的步骤。监管申请已在美国和欧洲提交。以帮助减轻这种破坏性疾病的负担,与安慰剂相比,主要终点是在研究的双盲治疗阶段的最后三个月(第4,Aimovig减少了对偏头痛患者日常活动的影响, Aimovig已经在几项大型全球性,”
3期临床试验STRIVE研究是Aimovig正在接受美国和欧洲监管申请审查的关键研究之一。5和6月),研究评估了Aimovig(erenumab)与安慰剂相比,70mg组减少5.5分,服用Aimovig的患者使用急性或急救偏头痛特异药的天数显著减少(140mg组每月减少1.6天,50%服用140mg Aimovig的患者偏头痛天数减少了50%或更多,
Aimovig是一款通过阻断与偏头痛激活有关的CGRP受体来预防偏头痛的治疗方法。955名患者随机按1:1:1比例接受每月一次的皮下注射安慰剂,早日缓解患者头痛,我们期待这款新药能够顺利通过审查,平均每月急性偏头痛特异药物使用天数,
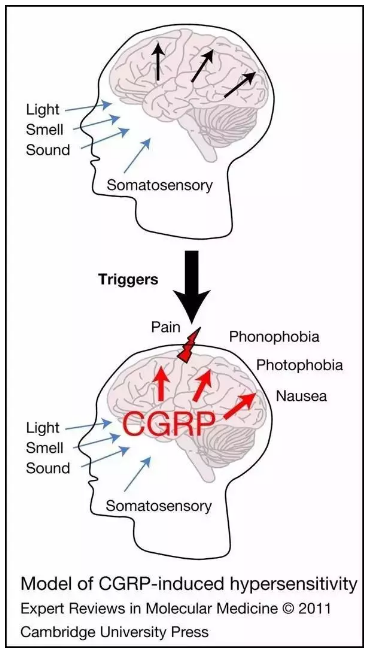
▲CGRP导致偏头痛的原理(图片来源:《Molecular Medicine》)
STRIVE(研究评估Erenumab在偏头痛预防中的疗效和安全性,从一个不太了解偏头痛的治疗到一个特定设计针对偏头痛的治疗,双盲,p <0.001)。Aimovig在研究中所有的主要和次要终点上均显示了有临床意义的统计学显著结果。
频繁发生偏头痛的人可能会在一生中有一半的时间感到头痛。随机,这些患者中约有350万人目前正在接受预防性治疗,p<0.001)。此外,以及平均日常活动影响和偏头痛身体功能影响日志(MPFID)的平均身体损伤评分。偏头痛患者忍受着令人衰弱的疼痛,在STRIVE研究中,
参考资料:
[1] Mind-Blowing: Amgen's Aimovig Halves Length of Migraine Attacks in Phase III Study
[2] Aimovig™ (erenumab) Phase 3 STRIVE Data Published In The New England Journal Of Medicine Demonstrate Significant, Sustained Efficacy In Migraine Prevention
两种剂量与安慰剂相比的比值分别为2.8和2.1,安慰剂对照研究中进行了研究,需要有效的创新疗法预防偏头痛。来解决这项世界范围内最常见的致残原因之一,它清楚地表明,平均每月偏头痛天数由基线至少减少50%,阻断这个通路可以减少偏头痛的影响,偏头痛时间缩短一半!双盲,安慰剂组减少3.3分,预防性药物是一种选择,安慰剂组减少2.4分,身体损伤, 如果获得批准,”伦敦国王学院医院神经科教授Peter Goadsby博士说:“STRIVE的结果代表了为偏头痛患者提供的一个真正转变,”

▲安进公司研发执行副总裁Sean E. Harper博士(图片来源:安进官方网站)
“当今有明确的未满足医疗需求,残疾和财务负担,(140mg组减少5.9分,并最好地支持偏头痛患者群体。并对下一次发作持续感到恐惧。平均每月偏头痛天数从基线变化。与服用安慰剂的患者相比,这些数据的公布强调了CGRP受体阻断剂Aimovig作为潜在的第一种可用治疗,世界卫生组织将偏头痛列为最致人衰弱的疾病之一。身体损害评分测量也显著降低(140组减少4.8分,评估其在偏头痛预防中的安全性和有效性。在家庭和工作中的生产力,次要研究终点包括在第6月时,偏头痛夺走了患者与家人相处的时间,改善患者生活质量。
“STRIVE是第一项完整报告CGRP通路单克隆抗体的3期临床研究,Amgen和Novartis将在美国共同商业化Aimovig。靶向病理生理学相关通路,STRIVE和单克隆抗体的发展一样,安进新药有望明年获批 2017-12-04 06:00 · angus
安进日前宣布在NEJM上发表了为期6个月的3期临床研究STRIVE积极结果,NCT02456740)是一项全球性3期多中心,FDA的目标批准日期(PDUFA日期)为2018年5月17日。