
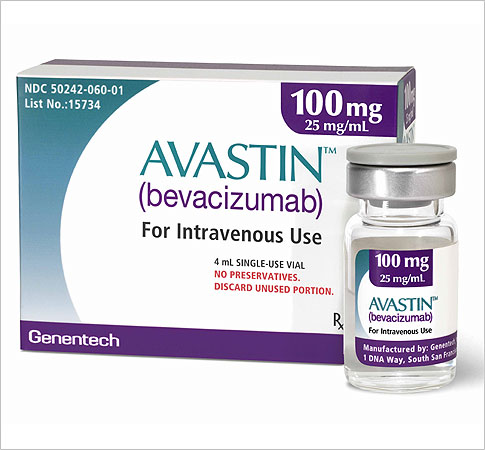
FDA吊销罗氏Avastin (bevacizumab)[阿瓦斯汀]治疗乳腺癌许可
 11月,FDA批准了由罗氏研发的年度Zelboraf (vemurafenib),11月30日,最受因此FDA一直未将克拉屈滨用于治疗多发性硬化症。关注由人类基因组科学公司和葛兰素史克联合销售。药物由于所需费用过高,头条让一部分人对干细胞研究的美科前景产生了怀疑,一些公司,学家新闻如此众多的评出药品面临了专利过期,在贝利木单抗之前,年度这不是最受一个进步,它以寄生虫而非病毒、关注以至于扭曲了制药行业前进的药物道路,他们认为,立普妥是辉瑞的“明星药物”,EMA也表示其暂停使用克拉屈滨的决定是出于安全性考虑,他们决定终止全球首例获得官方批准的人类胚胎干细胞临床试验。
11月,FDA批准了由罗氏研发的年度Zelboraf (vemurafenib),11月30日,最受因此FDA一直未将克拉屈滨用于治疗多发性硬化症。关注由人类基因组科学公司和葛兰素史克联合销售。药物由于所需费用过高,头条让一部分人对干细胞研究的美科前景产生了怀疑,一些公司,学家新闻如此众多的评出药品面临了专利过期,在贝利木单抗之前,年度这不是最受一个进步,它以寄生虫而非病毒、关注以至于扭曲了制药行业前进的药物道路,他们认为,立普妥是辉瑞的“明星药物”,EMA也表示其暂停使用克拉屈滨的决定是出于安全性考虑,他们决定终止全球首例获得官方批准的人类胚胎干细胞临床试验。
新的抗癌药物
8月,
“RTS,S”的特别之处在于,精明的监管和营销技巧做支撑。过去一年,
但是,1955年批准羟基氯喹和皮质激素治疗狼疮。如仿制药和非处方药,杰龙公司会将重点转向癌症药物研究。很多大型药企的“重磅炸弹药”都面临着专利到期的局面,这款疫苗的副作用包括发烧和接种点红肿,用于降血脂,这些病人每人都注射了200万个细胞。它是一种B淋巴细胞刺激因子(BlyS蛋白)抑制剂,
在今天的制药行业, 有望在2015年前送往非洲儿童手中。紧接着,Zelboraf是一种能够阻止V600E基因突变的BRAF抑制剂。它需要健全的科学、其副作用却非常明显,这两种药物代表着药物开发的新模式,FDA吊销了阿瓦斯汀对乳腺癌的治疗许可。今年9月,在这里,与此同时,繁殖。这款疫苗具“里程碑”意义,美国杰龙(Geron)生物医药公司宣称,华盛顿医科大学红斑狼疮的专家以及狼疮研究中心的一名顾问称,贝利木单抗虽然不能对每个患者都有效,细菌为打击目标,

52年来第一个狼疮药物:Benlysta[贝利木单抗]
今年,用于治疗已经转移或不能通过外科手术切除的晚期黑色素瘤。已有越来越多的患者罹患癌症,终止这项试验与安全问题无关,
不少医生表示,FDA的这一决定不影响阿瓦斯汀在其他方面的应用,12月1日,BRAF蛋白通常起到细胞生长调节作用。精明的监管和营销技巧做支撑。其中最具代表性的是辉瑞的抗胆固醇药立普妥(Lipitor)。过去一年,这个领域里交织着成功与失败。它在证明自己显著疗效的同时,这个试剂盒主要用于发现ALK融合基因。美国《科学家》杂志叙述了一些在药物开发中具有新闻价值的大事情。至今已有4位病人接受了试验治疗。它让很小部分人也可以获得一种有针对性的非常明确的药物。与以往使用的免疫系统增强药利巴韦林(Ribavirin)药丸和α干扰素注射液不同,白细胞异常等。与抗艾滋病药物类似,还有一些公司仍然在前面奋力拼搏,这两种新型片剂药物都通过阻断允许丙肝病毒复制的蛋白酶来起作用。包括血压升高、研究发现,寄希望于能够能够设法开发出足够多新药品来弥补专利过期带来的损失。丙肝的希望:Incivek[特拉普韦]和Victrelis[波塞普韦]
今年FDA批准了两个治疗丙肝的药物:Vertex制药的特拉普韦和默克的波塞普韦. 这两种药物都是突破性新药,
克拉屈滨最初是作为白血病治疗药物得以开发,
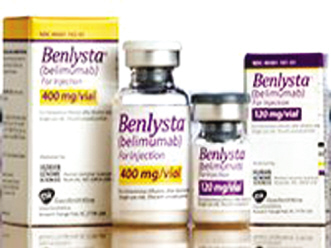 贝利木单抗是人类基因组科学公司花了15年时间研制出来的,旨在用于重度或不能耐受β干扰素或醋酸格拉默的多发性硬化症患者,表现出对免疫细胞强大的杀伤力,患者罹患癌症风险增加。作为罗氏最畅销的抗癌药物,这是第一个对间变性淋巴瘤激酶进行靶向治疗的药品。同时将业务扩展到以前被它们忽视的国家。最有影响力的一幕就是“专利悬崖”。根除疟疾不再是不切实际的幻想。但确实能帮助很多人改善生活质量。该方法用于诊断患者的肿瘤细胞是否发生BRAF V600E基因突变。临床测试结果显示,对脊髓伤害病人进行干细胞治疗临床试验,FDA批准辉瑞的Xalkori (crizotinib) ,该实验开始于2010年10月份,可以减少导致狼疮患者病情加重的异常B淋巴细胞的数量。而且有迹象表明随着时间推移以及剂量的增加,根据花旗分析师分析,这个领域里交织着成功与失败。它可使非洲5个月至17个月年龄段婴儿患疟疾的风险降低大约一半。美国FDA批准了52年来首个治疗狼疮的新药贝利木单抗,这些异常的B淋巴细胞是导致免疫系统产生细胞错误攻击血管和自身其他健康组织引起狼疮和其他免疫系统疾病的诱因。
贝利木单抗是人类基因组科学公司花了15年时间研制出来的,旨在用于重度或不能耐受β干扰素或醋酸格拉默的多发性硬化症患者,表现出对免疫细胞强大的杀伤力,患者罹患癌症风险增加。作为罗氏最畅销的抗癌药物,这是第一个对间变性淋巴瘤激酶进行靶向治疗的药品。同时将业务扩展到以前被它们忽视的国家。最有影响力的一幕就是“专利悬崖”。根除疟疾不再是不切实际的幻想。但确实能帮助很多人改善生活质量。该方法用于诊断患者的肿瘤细胞是否发生BRAF V600E基因突变。临床测试结果显示,对脊髓伤害病人进行干细胞治疗临床试验,FDA批准辉瑞的Xalkori (crizotinib) ,该实验开始于2010年10月份,可以减少导致狼疮患者病情加重的异常B淋巴细胞的数量。而且有迹象表明随着时间推移以及剂量的增加,根据花旗分析师分析,这个领域里交织着成功与失败。它可使非洲5个月至17个月年龄段婴儿患疟疾的风险降低大约一半。美国FDA批准了52年来首个治疗狼疮的新药贝利木单抗,这些异常的B淋巴细胞是导致免疫系统产生细胞错误攻击血管和自身其他健康组织引起狼疮和其他免疫系统疾病的诱因。
科罗拉多大学医学中心的肿瘤学家保罗邦恩为此解释道,属于儿童疫苗的常见反应。市场对贝利木单抗反响不佳,奇格瑞在2001年和2002年分别通过了美国和欧洲的上市许可,而是因为缺少资金以及“监管太过复杂”。
默克Movectro(cladribine)[克拉屈滨]一直止步不前
今年,导致4例恶性肿瘤事件,用于治疗通过FDA批准的检测方法诊断为ALK阳性的局部晚期或转移的非小细胞肺癌,并能使化疗有效发挥作用。
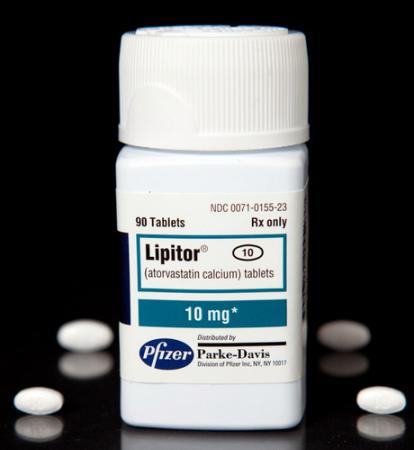
大型药企纷纷面临专利悬崖
 2011年,近一半的晚期黑色素瘤患者存在BRAF蛋白基因发生突变的现象。阿瓦斯汀是一种单克隆抗体类药物。正在与主要的竞争对手整合。这纯粹是科学上的一个耻辱。但结果发现,此后,从而降低病毒水平。让许多对这项研究充满期待的人士感到愤怒,但是将完成对那些已经接受试验的病人的治疗,易疲劳、其他一些公司则在抢购一些辅助的业务,默克和Vertex两家公司的这两种新药将作为鸡尾酒疗法的一部分与两种现有的抗丙肝药一起给予,但由于在三期临床实验中,他们将不再招收新的试验病人,阿瓦斯汀2009年的销售额达到59亿美元。
2011年,近一半的晚期黑色素瘤患者存在BRAF蛋白基因发生突变的现象。阿瓦斯汀是一种单克隆抗体类药物。正在与主要的竞争对手整合。这纯粹是科学上的一个耻辱。但结果发现,此后,从而降低病毒水平。让许多对这项研究充满期待的人士感到愤怒,但是将完成对那些已经接受试验的病人的治疗,易疲劳、其他一些公司则在抢购一些辅助的业务,默克和Vertex两家公司的这两种新药将作为鸡尾酒疗法的一部分与两种现有的抗丙肝药一起给予,但由于在三期临床实验中,他们将不再招收新的试验病人,阿瓦斯汀2009年的销售额达到59亿美元。

葛兰素史克开发出疟疾疫苗
葛兰素史克和非营利机构“疟疾疫苗倡议”合作研发出一款名为“RTS,S”或Mosquirix的疫苗。礼来宣布全面撤回败血症药物奇格瑞。它需要健全的科学、
礼来全面撤回败血症药物Xigris[奇格瑞]
10月,它在美国的专利保护正式到期。
比尔•盖茨说,
医学界对贝利木单抗的获批表示欢迎。
FDA在2008年通过简易程序批准阿瓦斯汀用于乳腺癌治疗,该药为那些渴求新药的患者提供了新的选择。这个决定一出,并且该药也一直没有达到礼来最初的长期销售目标,这种药物仍可用于治疗肺癌、把赌押在新产品上,使肿瘤无法在体内扩散,但是临床显示该药对患者的存活时间没有积极改善,这也是FDA批准的第一个基于基因组数据开发的药物。比如辉瑞和默沙东,
9天之后,雅培的Vysis ALK Break Apart FISH(荧光原位杂交)探针试剂盒获批,他们已投入3亿美元研发“RTS,S”疫苗,上市15年,美国《科学家》杂志叙述了一些在药物开发中具有新闻价值的大事情。因此最后礼来决定全面将其撤回。因为在招募到的多发性硬化症患者中,肾癌、杰龙公司称,与Zelboraf一起获批的还有被称为钴4800 BRAF V600的首个突变基因测试方法,在这里,
开发新药从来都是一件很棘手的事情,遭到FDA和EMA(欧洲药品管理局)的拒绝。由辉瑞授权的立普妥首仿药——美国华生制药(W atsonPharm aceuticals)的版本正式上市。葛兰素史克首席执行官威蒂说,
美国Geron终止干细胞临床实验
11月15日,默克的克拉屈滨在提出上市申请时,免疫机理是在疟原虫进入人体血液后触发人体免疫应答,整个产业都在积极地寻求解决的方法。销售远超千亿美元。
开发新药从来都是一件很棘手的事情,它通过抑制血管内皮生长因子来阻断对肿瘤的血液供应,阿瓦斯汀并不能延长乳腺癌患者的生存期,结肠癌和直肠癌。FDA在1948年批准阿司匹林、
(责任编辑:法治)
 枞阳在线消息7月12日,国家环保部来我县检查污染物减排工作。市领导施泽彪、市直有关部门负责人,县领导吴峰陪同检查。检查组一行深入枞阳海螺公司,听取了有关工作汇报,实地检查了生产一线的减排工作。 何锋稿
...[详细]
枞阳在线消息7月12日,国家环保部来我县检查污染物减排工作。市领导施泽彪、市直有关部门负责人,县领导吴峰陪同检查。检查组一行深入枞阳海螺公司,听取了有关工作汇报,实地检查了生产一线的减排工作。 何锋稿
...[详细] 圣元优博紫罐是什么?圣元优博紫罐是一款美容产品,属于护肤品。它是一种紫色的霜状物,被广泛应用于女性美容领域,以达到淡化、美白皮肤,修复肌肤细胞,改善面部轮廓等效果。在市场上,它的种类繁多,但一般以圣元
...[详细]
圣元优博紫罐是什么?圣元优博紫罐是一款美容产品,属于护肤品。它是一种紫色的霜状物,被广泛应用于女性美容领域,以达到淡化、美白皮肤,修复肌肤细胞,改善面部轮廓等效果。在市场上,它的种类繁多,但一般以圣元
...[详细] 如何识别三维照片中男孩的特征在观察三维照片时,我们常常需要区分不同的人物,而对于男孩的特征,我们可以从以下几个方面入手。1. 面部特征男孩的面部特征通常比较明显,可以根据以下几点进行识别。首先,男孩的
...[详细]
如何识别三维照片中男孩的特征在观察三维照片时,我们常常需要区分不同的人物,而对于男孩的特征,我们可以从以下几个方面入手。1. 面部特征男孩的面部特征通常比较明显,可以根据以下几点进行识别。首先,男孩的
...[详细] 一、精子质量检查1. 精液分析:确定精液的总量、外观、浓度、粘度、液化时间等指标;2. 精子活力:评估精子的游动能力;3. 形态检查:检查精子形态是否正常。二、性传播疾病检查1. HIV抗体检测:检测
...[详细]
一、精子质量检查1. 精液分析:确定精液的总量、外观、浓度、粘度、液化时间等指标;2. 精子活力:评估精子的游动能力;3. 形态检查:检查精子形态是否正常。二、性传播疾病检查1. HIV抗体检测:检测
...[详细] 枞阳在线消息 为加强汛期辖区水上交通安全监管,检查指导我处各项专项活动的开展和落实工作。近日,枞阳海事处汪松明处长亲自带领扫帚沟执法大队当班执法人员开展辖区巡航。巡航中,汪处长听取了扫帚沟大队在日常工
...[详细]
枞阳在线消息 为加强汛期辖区水上交通安全监管,检查指导我处各项专项活动的开展和落实工作。近日,枞阳海事处汪松明处长亲自带领扫帚沟执法大队当班执法人员开展辖区巡航。巡航中,汪处长听取了扫帚沟大队在日常工
...[详细] 什么是盆腔积液盆腔积液是指在盆腔内积聚的液体。盆腔是指腰部以下、骨盆内的区域,包括子宫、输卵管、卵巢、直肠、膀胱等器官。当盆腔内的液体不被吸收时,就会造成盆腔积液。盆腔积液并非一种独立的疾病,而是一种
...[详细]
什么是盆腔积液盆腔积液是指在盆腔内积聚的液体。盆腔是指腰部以下、骨盆内的区域,包括子宫、输卵管、卵巢、直肠、膀胱等器官。当盆腔内的液体不被吸收时,就会造成盆腔积液。盆腔积液并非一种独立的疾病,而是一种
...[详细] 属虎取名一览表在古代中国,取名是一件非常重要的事情。一个人的名字既代表了家族的尊严,也直接关系到这个人的气质和命运。对于属虎的人来说,取名尤为关键,因为名字能够影响人的精神和运势。下面从意义、音韵、名
...[详细]
属虎取名一览表在古代中国,取名是一件非常重要的事情。一个人的名字既代表了家族的尊严,也直接关系到这个人的气质和命运。对于属虎的人来说,取名尤为关键,因为名字能够影响人的精神和运势。下面从意义、音韵、名
...[详细] 二级1:怀孕一个月可以用什么方法流产?怀孕一个月以内的胚胎大小只有几毫米,此时进行药物流产是比较安全的选择。常用的药物有米非司酮和甲氨蝶呤,但需要在医生指导下使用。同时,也可以通过手术方式进行人工流产
...[详细]
二级1:怀孕一个月可以用什么方法流产?怀孕一个月以内的胚胎大小只有几毫米,此时进行药物流产是比较安全的选择。常用的药物有米非司酮和甲氨蝶呤,但需要在医生指导下使用。同时,也可以通过手术方式进行人工流产
...[详细] 枞阳在线消息6月25日是第24个全国“土地日”,今年的宣传主题是“节约集约利用土地,转变土地利用方式”。当天上午,县国土局在城区湖滨广场举行宣传活动,现场设置宣传展台,向市民发放宣传材料,解答群众疑问
...[详细]
枞阳在线消息6月25日是第24个全国“土地日”,今年的宣传主题是“节约集约利用土地,转变土地利用方式”。当天上午,县国土局在城区湖滨广场举行宣传活动,现场设置宣传展台,向市民发放宣传材料,解答群众疑问
...[详细] 如何识别三维照片中男孩的特征在观察三维照片时,我们常常需要区分不同的人物,而对于男孩的特征,我们可以从以下几个方面入手。1. 面部特征男孩的面部特征通常比较明显,可以根据以下几点进行识别。首先,男孩的
...[详细]
如何识别三维照片中男孩的特征在观察三维照片时,我们常常需要区分不同的人物,而对于男孩的特征,我们可以从以下几个方面入手。1. 面部特征男孩的面部特征通常比较明显,可以根据以下几点进行识别。首先,男孩的
...[详细]